徐惠绵教授点评|影像学联合ctDNA监测潜在可切除
执笔整理:赵长林教授
大连大学附属新华医院 大连结肠与直肠癌诊疗基地
本文为作者授权医脉通发布,未经授权请勿转载。
本病例主要针对潜在可切除结直肠癌肝转移(CRLM)转化治疗的相关问题展开理论与临床实践相结合的全面系统剖析。全程包括潜在可切除CRLM转化治疗获益指标筛选,转化治疗最佳方案的运用,优化了影像学与ctDNA对疗效动态评估及复发监测指标。本期隆重推出我国胃肠肿瘤诊疗领域的顶级专家,著名的胃肠肿瘤外科大咖徐惠绵教授对病例做精彩的点评。病例链接:实战病例 | 影像学联合ctDNA监测潜在可切除CRLM综合治疗效果及预后。

徐惠绵教授
●国家二级教授,国务院特殊津贴专家,博士生导师,大连大学客座教授
●现任中国医科大学附属第一医院肿瘤中心主任
●中华医学会肿瘤学分会第十一届主任委员
●中国抗癌协会胃癌专业委员会主任委员等学术任职
●中央保健委员会会诊专家
●长期致力于探索肿瘤转移规律及优化临床规范诊治的工作,为提高我省乃至全国肿瘤防治水平做出突出贡献
●曾获第十届中国医师奖、辽宁省政府优秀专家、首届辽宁名医等荣誉称号
●先后主持、承担根据自然科学基金项目和“863”、“973”等国家级与省部级科研项目19项发表国内核心期刊论文161篇,SCI收录论文93篇,累计影响因子300余点
●主编胃癌专著2部
●2001年、2006年两次荣获国家科技进步二等奖和多项省部级科技进步奖励
徐惠绵教授点评
结直肠癌患者在初次诊断时同时存在肝脏转移瘤的患者约占15%~20%。潜在可切除CRLM患者约占70%~80%。针对潜在可切除CRLM,通过有效的转化治疗可使这些患者转化为可切除并能够达到R0切除或无疾病状态(NED),5年累积生存率可达到45%~50%,显著优于姑息治疗。但是,肝转移切除术后60%~70%的患者会发生局部复发或新发转移,出现复发、转移的患者长期生存显著缩短。
CRLM的特点是转移灶多发多见,大小不一,生物学特征各异。目前的常规影像学腹部CT增强扫描不能发现肝脏全部转移灶,如果在手术前或术中不能发现CRLM患者的微小病灶和新辅助或转化治疗后的消失病灶,肝转移切除术后的残留病灶就会发生局部复发或转移。
随着影像诊断技术的进步,增强MRI、肝脏钆塞酸二钠增强MRI(普美显/EOB-MRI)联合弥散加权成像(DWI)、声诺维(SonoVue)超声造影、术中示卓安超声造影(Sonazoid-IOUS)从不同角度提高了CRLM诊断的准确性和综合治疗效果评价的准确性。
对于CRLM患者的肝脏病灶,准确地定性、定量和定位诊断可以确保R0切除,不漏掉微小病灶或消失病灶,不残留病灶,最大限度的保留肝实质。因此,根据诊断的需要和治疗目标,合理选择或联合应用现代影像学技术是非常重要和十分有益的。
ctDNA来自肿瘤细胞的体细胞突变。组织ctDNA的常见突变与血浆ctDNA的常见突变高度一致,敏感性75%,特异性90%。ctDNA动态变化与肿瘤突变负荷(TMB)的变化一致。在胃肠癌、黑色素瘤、肺癌和膀胱癌中TMB最高(图1可放大)。
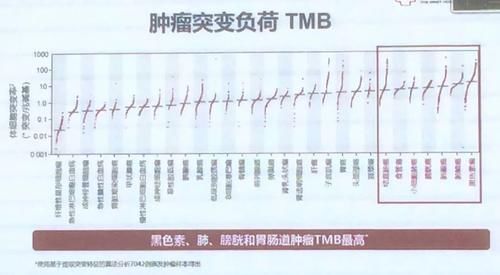
图1 肿瘤体细胞突变率
临床研究显示,约有91.7%的上述肿瘤在综合治疗后出现了血浆TMB水平的显著下降。在临床治疗过程中,对连续采集的血浆样本通过二代测序(NGS)方法检测分析初始TMB的结果显示,ctDNA动态变化与TMB一致。初步研究结果也证实,ctDNA与CRLM患者预后相关,可监测CRLM术后微小残留病变(MRD)预测肿瘤复发,是无复发生存期(RFS)和总生存期(OS)的独立预后因子。
2019年5月,JAMA Oncoloy杂志连续刊登两篇有关ctDNA在预测非转移性结直肠癌根治术后复发和预后的研究。2021 ASCO GI 口头报告了ctDNA分析可更早发现结直肠癌术后高危人群。随着ctDNA在肿瘤诊疗领域的深入研究和实践,ctDNA有可能成为肿瘤综合诊疗的新型评价指标 (图2可放大)。
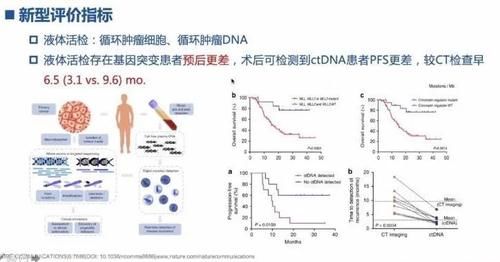
图2 ctDNA肿瘤综合诊疗的新型评价指标
由于受所处地域和医院技术、条件及设备所限,目前国内各地区结直肠癌多学科规范化综合诊疗水平和MDT的效应参差不齐,整体诊疗水平和MDT的效应有待进一步提升。大力倡导国内肿瘤中心之间的技术合作和临床研究的合作,在确保结直肠癌多学科规范化综合诊疗和患者知情的前提下,开展具有探索性的临床研究具有重要的临床意义。